El
átomo es la partícula más pequeña e indivisible de un elemento químico
que contiene íntegras sus propiedades. Su estudio constituye la base de
la física y la química contemporáneas. Los átomos de un elemento se
pueden combinar con los de otro para formar la unidad más pequeña de un
cuerpo compuesto, llamada molécula, que, a su vez, se une con otras para
formar los propios cuerpos compuestos.
 Dalton acuñó los conceptos de peso atómico y molécula (formada por la
combinación de varios átomos) y elaboró la primera tabla de elementos en
1805. Posteriormente, las nociones de átomo y moléculas no dejaron de
precisarse y concretarse. La clasificación periódica de los elementos de
Mendeleiev (1869) vino a coronar los esfuerzos de los químicos y a
anunciar que todo el Universo puede estar formado sólo por un centenar
de átomos diferentes.
Dalton acuñó los conceptos de peso atómico y molécula (formada por la
combinación de varios átomos) y elaboró la primera tabla de elementos en
1805. Posteriormente, las nociones de átomo y moléculas no dejaron de
precisarse y concretarse. La clasificación periódica de los elementos de
Mendeleiev (1869) vino a coronar los esfuerzos de los químicos y a
anunciar que todo el Universo puede estar formado sólo por un centenar
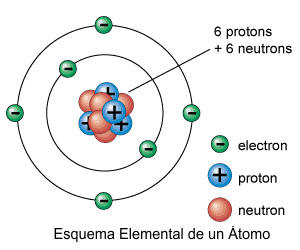
de átomos diferentes.Todo átomo está constituido por tres partes: una parte eléctricamente positiva, formada por losprotones; otra eléctricamente negativa, compuesta por electrones, y una tercera integrada por minúsculas partículas neutras denominadas neutrones. La carga electrónica del protón y la del electrón son iguales y contrarias; como los átomos suelen existir en forma neutra, el número de electrones de un átomo debe ser igual al de protones. Los electrones ocupan el espacio más externo del átomo; y los protones se sitúan en el centro, y, con los neutrones, constituyen el núcleo.
Los electrones y los protones de todos los elementos químicos son
iguales, por lo que éstos se diferencian por el número de protones, de
neutrones y de electrones presente, mi su interior.
