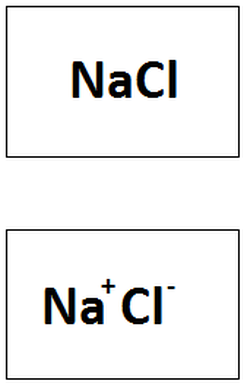Enlaces Químicos
Un enlace químico corresponde a la fuerza que une o enlaza a dos átomos, sean estos iguales o distintos. Los enlaces se pueden clasificar en tres grupos principales: enlaces iónicos, enlaces covalentes y enlaces dativos.
Los enlaces se producen como resultado de los movimientos de los
electrones de los átomos, sin importar el tipo de enlace que se forme.
Pero no cualquier electrón, puede formar un enlace, sino solamente los
electrones del último nivel energético (más externo). A estos se les
llama electrones de valencia.
En este capítulo analizaremos las características de cada tipo de
enlace, como también veremos diferentes maneras de representarlos en el
papel. Partiremos definiendo lo que es un enlace iónico.
- Enlace iónico: Un enlace iónico se puede definir como la fuerza que une a dos átomos a través de una cesión electrónica.
Una cesión electrónica se da cuando un elemento electropositivo se une
con un elemento electronegativo. Mientras mayor sea la diferencia de
electronegatividad entre los elementos, más fuerte sera el enlace
iónico. Se empieza a considerarque dos átomos están unidos a través de
un enlace iónico cuando sudiferencia de electronegatividad es superior a 1.7. Un ejemplo de un compuesto unido a través de enlace iónico se muestra en la Imágen 27, mientras que en la Imágen 28 se ve algunas maneras de escribir compuestos unidos mediante este tipo de enlace.
Formas de escribir una molécula que está unida mediante un enlace Iónico.

- Enlace Covalente: El enlace covalente es la fuerza que une dos átomos mediante la compartición de un electrón por átomo. Dentro de este tipo de enlace podemos encontrar dos tipos: el enlace covalente polar y el enlace covalente apolar.
El primer sub-tipo corresponde a todos aquellos compuestos en donde la
diferencia de electronegatividad de los átomos que lo componen va desde 0 hasta 1.7 (sin
considerar el 0). Los compuestos que son polares se caracterizan por
ser asimétricos, tener un momento dipolar (el momento dipolar es un
factor que indica hacia donde se concentra la mayor densidad
electrónica) distinto a 0, son soiubles en agua y otros solventes
polares, entre otras características. Dos ejemplos se ven en la Imágen 29 (a) y en la Imágen 29 (b),
respectivamente. Por su parte, los compuestos que se forman por medio
de enlaces covalentes apolares, no presentan momento dipolar, la
diferencia de electronegativodad es igual a 0, son simétricos, son
solubles en solventes apolares (como el hexano), entre otras cosas. La
diferencia de electronegatividad cero se da cuando dos átomos iguales se
unen entre sí, como por ejemplo la molécula de Nitrógeno o la molécula
de Cloro (ver Imágen 30 (a) e Imágen 30 (b) respectivamente).
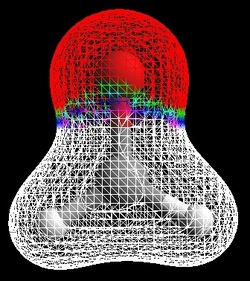
Densidades electrónicas en los siguientes compuestos polares: a) formaldehído (o metanal); b) 1,2-difluoretano.
El color blanco indica una escacez de electrones, de ahi vienen
respectivamente el color violeta, azul, verde y rojo (el cual indica
mayor densidad electrónica).
http://es.wikipedia.org/wiki/Enlace_qu%C3%ADmico